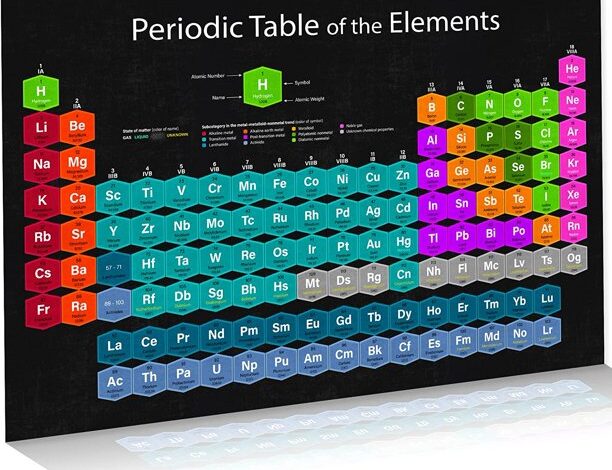
جدول تناوبی عناصر را بر اساس خواص دوره ای مرتب می کند که روندهای تکرار شونده در ویژگی های فیزیکی و شیمیایی هستند. این روندها را می توان صرفاً با بررسی جدول تناوبی پیش بینی کرد و با تجزیه و تحلیل آرایش های الکترونی عناصر قابل توضیح و درک است.
عناصر تمایل دارند تا الکترون های ظرفیتی را به دست آورند یا از دست بدهند تا به شکل گیری اکتت پایدار دست یابند. اکتت های پایدار در گازهای بی اثر یا گازهای نجیب گروه هشتم جدول تناوبی دیده می شوند. علاوه بر این فعالیت، دو گرایش مهم دیگر نیز وجود دارد.
اول، الکترون ها یکی یکی اضافه می شوند که از چپ به راست در یک دوره حرکت می کنند. همانطور که این اتفاق میافتد، الکترونهای خارجیترین پوسته جاذبه هستهای قویتری را تجربه میکنند، بنابراین الکترونها به هسته نزدیک تر می شوند و محکم تر به آن متصل می شوند.
دوم، با حرکت به سمت پایین یک ستون در جدول تناوبی، بیرونی ترین الکترون ها کمتر به هسته متصل می شوند. این به این دلیل اتفاق می افتد که تعداد سطوح انرژی اصلی پر شده (که از بیرونی ترین الکترون ها در برابر جاذبه به هسته محافظت میکنند) در هر گروه به سمت پایین افزایش می یابد. این روندها تناوب مشاهده شده در خواص عنصری شعاع اتمی، انرژی یونیزاسیون، میل ترکیبی الکترون و الکترونگاتیوی را توضیح می دهند.
عناصر در جدول تناوبی
جدول تناوبی نموداری از عناصر شیمیایی است که بر اساس عدد اتمی آنها سازماندهی شده اند. این جدول از 118 عنصر تشکیل شده است. هفتاد و دو مورد از این عناصر فلزی هستند. فلزات از نظر خواص فیزیکی و شیمیایی از غیر فلزات متمایز می شوند.
فلزات رسانای خوبی برای گرما و الکتریسیته هستند و چکش خوار و انعطاف پذیر هستند. نافلزات هادی ضعیف گرما و الکتریسیته هستند و شکننده هستند.
هیدروژن گازی بی رنگ، بی بو و بی مزه است. این عنصر سبک ترین عنصر در جهان است و غیرفلزی است. هیدروژن را می توان در آب یافت و در پیل های سوختی نیز استفاده می شود.
بحث بر سر فلز یا غیرفلز بودن هیدروژن سالهاست که وجود داشته است. برخی از دانشمندان معتقدند که هیدروژن یک فلز است زیرا می تواند با فلزات دیگر پیوند برقرار کند، در حالی که برخی دیگر می گویند که هیدروژن یک نافلز است زیرا خواص فلزات را ندارد. عوامل مختلفی وجود دارد که می تواند به شما کمک کند تصمیم بگیرید کدام طرف درست است. اولین عاملی که باید در نظر گرفت محل هیدروژن در جدول تناوبی است. هیدروژن در گروه 1A قرار دارد که معمولاً فلزات در نظر گرفته می شوند.
ویژگی جدول تناوبی
خواص تناوبی ویژگی های اتم هایی هستند که به طور منظم از چپ به راست در یک دوره و از بالا به پایین در یک گروه تغییر میکنند. خواص دوره ای مختلف عبارتند از: شعاع اتمی، انرژی یونیزاسیون، الکترونگاتیوی، میل الکترونی.
خواص شیمیایی و فیزیکی عناصر با پیکربندی پوسته ظرفیت آنها ارتباط دارد. پیکربندی پوسته ظرفیت هر دو عنصر در یک دوره معین مشابه نیست و به همین دلیل است که عناصر در یک دوره دارای خواص شیمیایی و فیزیکی متفاوتی هستند در حالی که تعداد پوسته های ظرفیت هر دو عنصر در یک گروه معین مشابه نیست. دلیل این است که عناصر یک گروه دارای خواص شیمیایی و فیزیکی متفاوتی هستند و به این ویژگی دوره ای می گویند.
اهمیت جدول تناوبی
طبقه بندی عناصر برای مطالعه خصوصیات فردی و روشی سیستماتیک برای سازماندهی دانش آنها در جستجوی عناصر بسیار ضروری است. ابتدا دوبرنیر مطالعه یک رابطه تناوبی را پس از آن آغاز کرد که مندلیف مسئول اولین جدول زمانی- تناوبی بود که اولین قانون تناوبی را به شرح زیر ساخته و منتشر کرد:
ویژگی عناصر تابع از وزن اتمی آنها است
پس از آن قانون تناوبی اصلاح شده مندلیف که عدد اتمی را مشخص می کند، ویژگی اساسی تری نسبت به جرم اتمی است و قانون تناوبی اصلاح شده به عنوان قانون تناوبی مدرن نام گذاری می شود که به شرح زیر است:
خواص فیزیکی و شیمیایی عناصر تابع تناوبی اعداد اتمی آنهاست
این قانون جدول تناوبی مندلیف را به جدول تناوبی مدرن تغییر می دهد. تفاوت های بیشتری بین جدول تناوبی مندلیف و جدول تناوبی مدرن ارائه شده در زیر وجود دارد.
فلز منگنز در گروه هالوژن قرار دارد. این عیوب توسط جدول تناوبی مدرن اصلاح می شوند. ویژگی اساسی برای متمایز کردن هر عنصر در جدول تناوبی مدرن، عدد اتمی است که ماهیت اصلی را برای تعیین خواص فیزیکی و شیمیایی عناصر نسبت به وزن اتمی می دهد.